 EN
EN
 EN
EN

专家简介 Expert Profile
郭红卫 Guo Hongwei 教授,博士生导师
现为中国营养学会常务理事﹐上海市营养学会名誉理事长﹐上海市学生营养与健康促进会副会长。历任上海市营养学会理事长、副理事长,上海市预防 医学会食品安全专业委员会主任委员。现任﹙或曾 任﹚《中华预防医学杂志》﹑《卫生研究》﹑《环境 与职业医学》﹑《中国食品卫生杂志》﹑《实用预防医学杂志》和《卫生毒理学杂志》编委。长期从事 营养与食品卫生学的教学和科研工作,主要研究方 向为营养与慢性疾病、霉菌毒素与健康。曾承担多 项国内外相关研究项目﹐已发表相关论文 130 余篇﹐主 编教材和专著 9 本,副主编 2 本,参编 10 本。所研 究项目曾获部委科技进步二等奖 1 项﹑三等奖 3 项。曾 获吴阶平医学研究 - 保罗·杨森药学研究三等奖﹑上 海市教委比翼双飞奖。获国家发明专利 1 项。
刘双江 Liu Shuangjiang 教授,博士生导师 博士,特聘教授
刘双江﹐博士﹐山东大学特聘教授、中国科学院微 生物研究所研究员,中国生物物理学会肠道菌群分会 会长、中国微生物学会环境微生物专业委员会副主任、 iMeta 主编﹑《微生物学报》执行主编﹑《生物工程学 报》副主编。曾任中国科学院微生物研究所第九届所长、 获得国家自然科学杰出青年基金项目、中国科学院百 人计划﹙海外优秀人才﹚项目支持、获得全国优秀科技 工作者称号。 主持并完成了科技部重点研发项目、国家自然科 学基金重大、重点和面上项目、科技部973课题和863 项目、中国科学院重大和重要研究项目。作为主要发 起人,提出中国微生物组研究计划,并主持了中国科 学院微生物组研究计划重点部署项目。研究领域为环 境微生物学和肠道微生物组,长期开展微生物的分离 培养、分类鉴定、生理生化、生态互作、遗传代谢和 应用转化等方面研究,发表学术论文300余篇。
冯 颖 Feng Ying 副主任技师
历任江苏省营养学会理事长,中国营养学会常务理事和监事等。现任江 苏省营保健食品审评专家。先后主持国家自然科学基金、国际合作等多项科 研项目,发表研究论文70余篇,SCI论文24篇。主编科普书1部,参编营养学 书籍9部。《中国居民膳食指南》﹑《中国居民膳食营养素参考摄入量DRIs》编 委。授权国家发明专利6项,获中国营养学会科技奖2项、南京市科技成果奖1 项、“中国营养学会百名英才奖”、“江苏省全民科学素质工作先进个人”等奖励。
华金中 Hua Jinzhong 教授、国家级注册营养师
上海三甲医院营养科副主任。现任中国营养学会老年营养分会委员,中国 老年保健医学会老年营养健康分会副主委,中国健康管理协会临床营养与健康 分会常务理事,中国营养保健食品协会特殊医学用途配方食品应用委员会常务 委员,中国食品科学技术学会益生菌分会理事,上海市营养学会副理事长,上 海药膳协会副理事长,上海市临床营养质控中心专委会委员等。从事临床营养 及老年营养工作 30 余年,主要研究方向为营养与代谢、常见慢病的营养防治 和营养健康促进。国内外期刊发表论文及科普 50 余篇,主编及参编教材、专 著及科普书籍 10 余本,所在团队曾获 2008 年上海市科技进步三等奖、2009 年教育部科技进步二等奖等。
伍佩英 Wu Peiying 副主任技师
曾任浙江省营养学会第四至第六届副理事长兼秘书长,连任中国营养学会 第四至第八届理事,浙江省营养学会监事长,第一、二届浙江省营养学会学生 营养与健康专业委员会主任委员。 擅长人体营养状况的评估、评价,各类健康管理的咨询、指导及效果评 估,膳(饮食)的分析与评价,营养及保健食品的开发、利用、制作与应用,营 养与健康的培训和指导。主编及参编教材、书籍十余部,刊登论文50余篇。承 担科技项目20余项、荣获科技进步奖项近10项。先后获得“全国营养科技工作 者、优秀科普先进个人”及“省级优秀科技、科协”及浙江大学、营养行业等奖项 30余项。
蔡云清 Cai Yunqing 教授,博士生导师
曾任上海三甲医院营养科主任。中国营养学会糖尿病营养专业委员会委员, 上海市食品安全风险评估专家委员会膳食营养专业委员会委员,上海市营养学会 理事,上海市临床营养质控中心专家委员,上海市食疗研究会理事等。长期从事 营养与慢性非传染性疾病的饮食调理和营养治疗,尤其是糖尿病(包括妊娠糖尿 病)、孕妇营养、高脂血症、肾脏病人、痛风病人、老年病人等的营养指导。主 持《糖尿病社区营养干预研究》﹑《β-葡聚糖对实验性代谢综合征的改善作用及 其机制研究》等研究,参与了《高血压的社区营养健康教育干预研究》。发表论 文数10篇,主编《更年期食谱》。
目录 Contents
1 肥胖挑战与肠道菌群的新视角
1. 1 肥胖 / 超重流行趋势
1. 2 传统减重方法的局限
1. 3 肠道菌群﹕人体代谢的“第二基因组”
1. 4 肥胖的精准分型﹕从宏观表征到微观机制
1. 5 肥胖分型与肠道菌群功能失调的内在联系
2 肠道菌群调控体重的六大机制
2. 1 肠道屏障功能维护与慢性炎症改善
2. 2 糖代谢调控的菌群-宿主对话
2. 3 脂代谢调控的多维度干预
2. 4 食欲与饱腹感的神经内分泌调控(一)
2. 5 食欲与饱腹感的神经内分泌调控(二)
2. 6 能量消耗与产热的菌群调控
2. 7 抑制营养吸收
3 益生菌靶向菌群体重管理法
3. 1 益生菌的定义与菌株特异性
3. 2 “靶向菌群体重管理法”的提出
3. 3 靶向菌群管理法的应用时序
3. 4 基于肥胖分型的精准靶向干预策略
4 结论与展望
PART 1 肥胖挑战与肠道菌群的新视角
1.1 肥胖 / 超重流行趋势
肥胖与超重已成为全球性的公共卫生 危机。世界卫生组织数据显示﹐ 2022 年全 球 18 岁及以上成人中约 16% 为肥胖﹐儿童 和青少年肥胖率也从 2% 增至 8%。在中国, 超重和肥胖问题同样严峻﹕ 2020 年数据显 示,成年人超重 / 肥胖率已达50.7% ﹐6-17 岁青少年为 19% ﹐ 6 岁以下儿童也达到 10.4%。这意味着每 2 个成人﹑ 5 个青少年 或 10 个儿童中就有 1 人面临超重或肥胖。
肥胖不仅是体态问题,更严重威胁健 康。高 BMI 是导致慢性非传染性疾病过 早死亡的重要风险因素﹐在 2 型糖尿病相关 的过早死亡中﹐ 55% 可归因于高 BMI。此 外﹐肥胖还显著增加心血管疾病、某些癌 症﹑骨关节炎和睡眠呼吸暂停等疾病风险。
1.2 传统减重方法的局限
传统的体重管理方法主要包括饮食控制、增加运动、药物治疗和手术干预。然而,这 些方法普遍存在局限性﹕饮食和运动依从性差、反弹率高;药物常伴有副作用;手术虽效 果显著,但侵入性高、存在手术风险和术后并发症。这些局限凸显了寻找更有效、更可持 续的体重管理策略的迫切性。
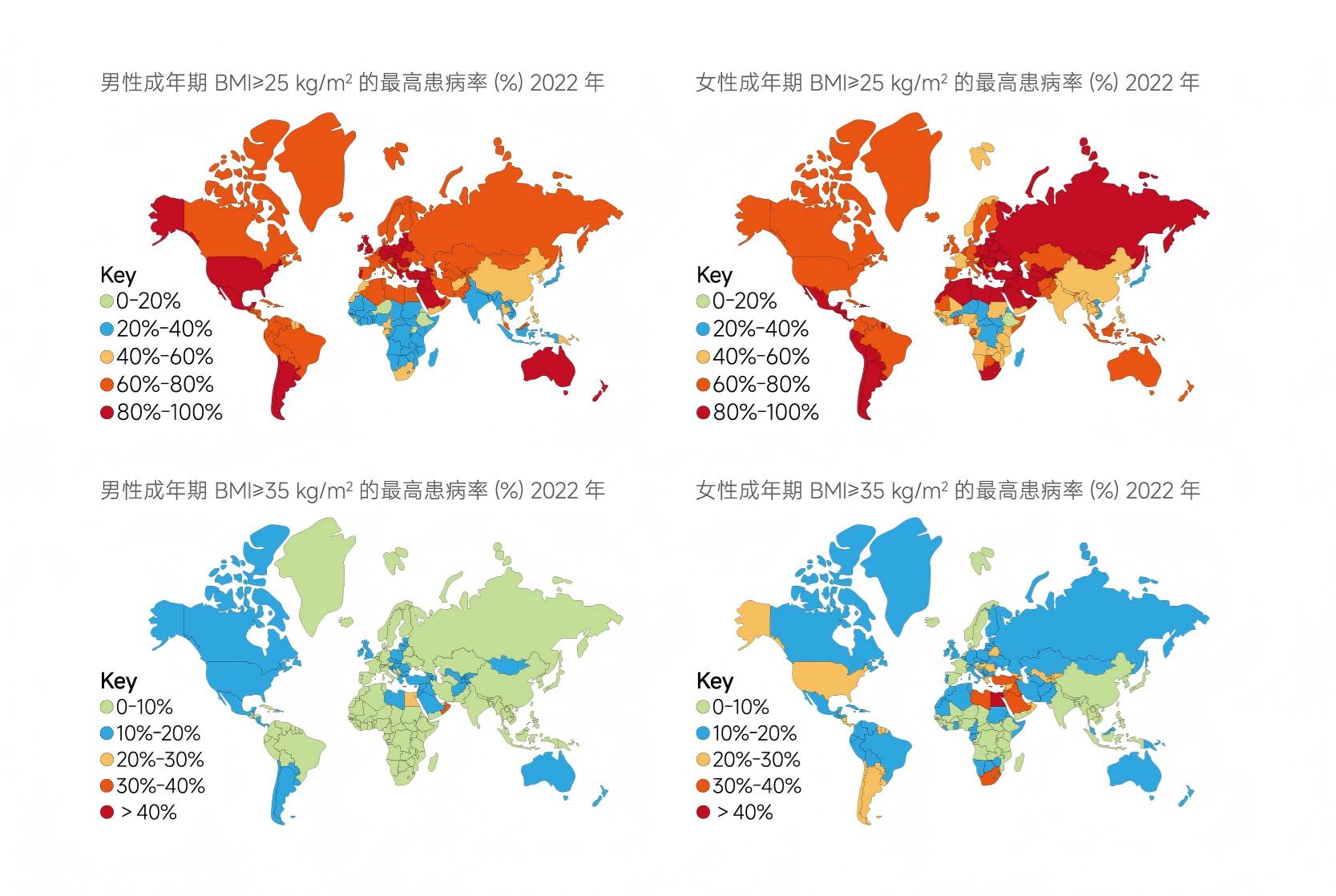 图 1 全球成人肥胖 / 超重患病率
图 1 全球成人肥胖 / 超重患病率
1.3 肠道菌群﹕人体代谢的“第二基因组”
人体肠道内寄居着数万亿微生物﹐其基因数 量是人类自身基因的100 多倍﹐被誉为 “第二基因 组”。肠道菌群不仅参与食物的消化吸收﹐更在 能量代谢﹑脂肪储存﹑免疫调节及炎症反应中发挥关键作用。
研究发现﹐肥胖个体的肠道菌群组成与 健康个体存在显著差异﹐由此提出 “肥胖菌群” 和 “瘦子菌群” 的概念。经典的双胞胎研究显 示﹐将肥胖者的肠道菌群移植给无菌小鼠﹐小 鼠体重和脂肪堆积显著增加;而移植瘦者的 菌群则无此效应。这直接证明了肠道菌群在 体重调控中的因果作用。
1.4 肥胖的精准分型:从宏观表征到微观机制
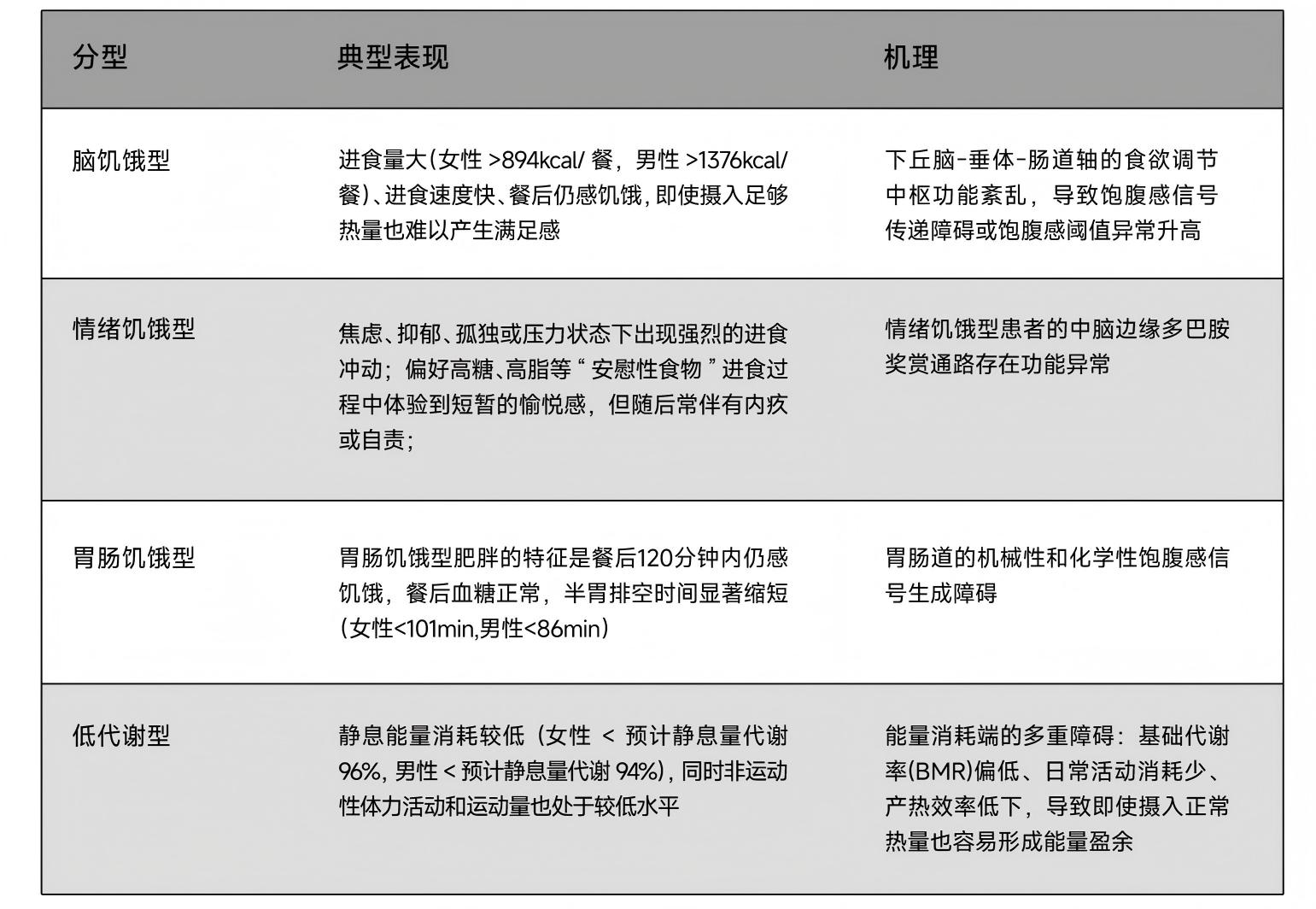
长期以来﹐肥胖被简单定义为BMI超标﹐但临床实践显示﹐相同的干预方案在不同个体身上效 果差异巨大。这种差异源于肥胖并非单一疾病﹐而是由不同病理生理机制导致的异质性综合征。 美国梅奥诊所提出了肥胖的四种病理生理分型:
1) 脑饥饿型﹕表现为进食量大、进食速度快、餐后仍感饥饿,源于下丘脑食欲调节中枢功能紊 乱,导致饱腹感信号传递障碍。
2) 情绪饥饿型﹕在焦虑、抑郁或压力下出现强烈进食冲动,偏好高糖高脂食物,与中脑边缘多 巴胺奖赏通路功能异常及5-HT系统失衡有关。
3) 胃肠饥饿型﹕餐后120分钟内仍感饥饿,半胃排空时间显著缩短,因胃肠道饱腹感信号生成 障碍,特别是肠道L细胞分泌GLP-1和PYY的能力减弱。
4) 低代谢型:静息能量消耗显著低于预计值,同时日常活动量低,基础代谢率偏低,与线粒 体功能减弱、UCP-1表达不足及胆汁酸代谢异常相关。
表 1 梅奥诊所肥胖分型及特征
1.5 肥胖分型与肠道菌群 功能失调的内在联系
更为关键的是,每种肥胖分型背后都存在特定的肠道菌群功能失调模式:
1) 脑饥饿型﹕肠-脑轴功能紊乱﹐菌群产GABA和调节5-HT的能力下降﹐导致神经递质失衡,同 时慢性炎症引发瘦素抵抗。
2) 情绪饥饿型﹕肠道菌群通过“肠-脑轴”双向通讯途径,利用神经递质、免疫反应和信号分子直 接影响大脑功能和情绪。
3) 胃肠饥饿型﹕产短链脂肪酸﹙SCFAs﹚的关键菌群﹙如双歧杆菌、拟杆菌﹚丰度显著降低,导致 GLP-1和PYY分泌不足﹐饱腹感信号减弱。
4) 低代谢型﹕产胆盐水解酶﹙BSH﹚的菌群﹙如乳杆菌﹑双歧杆菌﹚减少﹐次级胆汁酸生成不足, TGR5和FXR信号通路激活减弱,能量消耗下降。 这一分型体系将肥胖从单一的“能量过剩”转化为可精准识别、可靶向干预的不同病理状态,为个体化体重管理提供了科学依据。
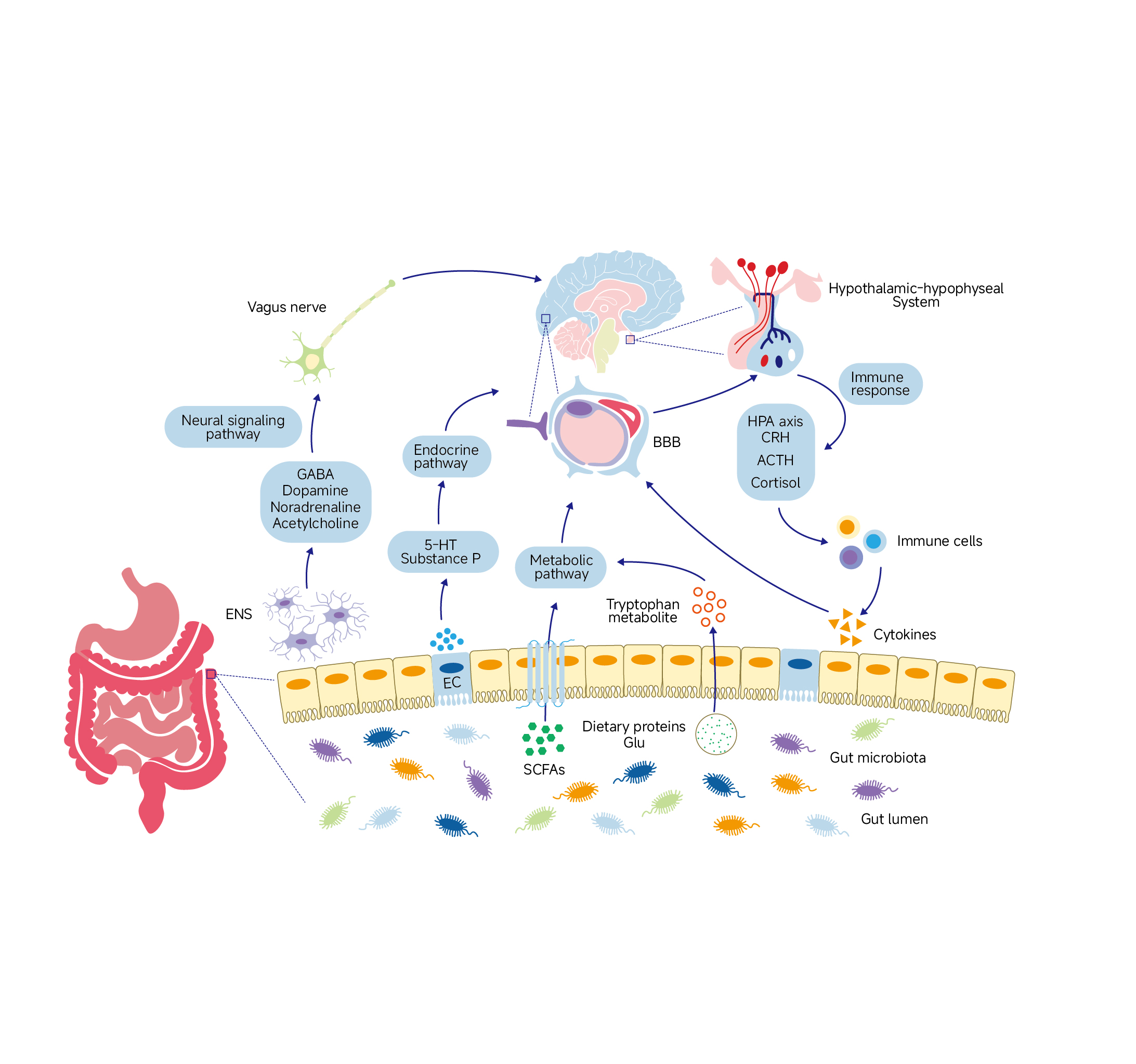 图 2 肠道菌群 - 脑 - 肠轴机制
图 2 肠道菌群 - 脑 - 肠轴机制
PART 2 肠道菌群调控体重的六大机制
2.1 肠道屏障功能维护与慢性炎症改善
低度慢性炎症是肥胖的核心病理特征﹐ 其源头正是功能受损的肠道屏障。肠道屏障 由四层构成﹕生物屏障﹙共生菌群﹚﹑化学屏障 ﹙黏液层﹚﹑免疫屏障﹙肠道相关淋巴组织﹚和物 理屏障﹙肠上皮细胞间的紧密连接﹚。 当菌群失调时,革兰氏阴性菌产生的 脂多糖﹙ LPS ﹚通过受损的肠道屏障进入血液,引发“代谢性内毒素血症”。LPS 与免疫 细胞表面的 TLR4 受体结合,激活 NF-κ B 通路﹐释放 TNF- α﹑ IL-6 等促炎因子。这 些因子进一步破坏紧密连接蛋白﹙如ZO-1﹑ Occludin ﹚,加剧肠漏,形成恶性循环。持 续的低度炎症干扰胰岛素信号传导,导致胰岛素抵抗。
不同肥胖分型的炎症特征存在差异:
1) 脑/情绪饥饿型:神经炎症干扰下丘脑瘦素信号,导致中枢食欲调控失常。
2) 胃肠饥饿型:肠道局部炎症抑制L细胞功能,减少GLP-1分泌。
3) 低代谢型:全身性炎症抑制线粒体功能和棕色脂肪产热,进一步降低代谢率。
2.2 糖代谢调控的菌群 - 宿主对话
菌群通过多种途径影响糖代谢:
1) 提高胰岛素敏感性﹕SCFAs﹙特别是丙 酸和丁酸﹚激活脂肪细胞和L细胞表面的 FFAR2/FFAR3受体,抑制脂肪分解,减少 游离脂肪酸释放,改善胰岛素敏感性;同时 通过抑制炎症,减少IRS-1的丝氨酸磷酸化, 保护胰岛素信号通路。
2) 抑制肝糖输出﹕SCFAs激活肠-脑-肝神 经回路﹐抑制肝脏糖异生关键酶﹙PEPCK﹑ G6Pase﹚的表达﹔次级胆汁酸激活TGR5受 体﹐促进GLP-1分泌﹐抑制胰高血糖素释放片。
3)促进肠促胰素分泌﹕SCFAs激活L细胞 FFAR2/3﹐触发GLP-1和PYY分泌;次级胆 汁酸激活TGR5同样促进GLP-1释放。
胃肠饥饿型肥胖的特征正是产SCFAs菌群缺 乏,导致GLP-1/PYY分泌受损,餐后血糖 波动剧烈﹙先高后低﹚﹐引发频繁饥饿感。
2.3 脂代谢调控的 多维度干预
菌群通过其代谢产物从多个维度调控脂代谢﹕
1) 抑制脂肪合成﹕次级胆汁酸激活肝脏FXR 受体﹐诱导SHP表达,抑制SREBP-1c﹙脂 肪合成总开关﹚;SCFAs激活AMPK,磷酸 化并抑制ACC﹙脂肪酸合成的限速酶)。
2) 促进脂肪分解与氧化﹕AMPK激活后,解 除对CPT1的抑制,促进脂肪酸进入线粒体 进行β-氧化;菌群调节去甲肾上腺素水平, 激活HSL﹙激素敏感性脂肪酶)。
3) 调节胆固醇代谢﹕菌群BSH将结合型胆汁 酸水解为游离型,促进粪便排泄,迫使肝脏 消耗胆固醇合成新的胆汁酸,从而降低血清 胆固醇。
低代谢型肥胖的核心缺陷即BSH活性不足, 导致次级胆汁酸生成障碍,FXR/TGR5信号 激活不足,AMPK活性降低,形成“易胖难 瘦”的体质。
2.4 食欲与饱腹感的神经内分泌调控(一)
菌群通过“肠-脑轴”深刻影响食欲:
1) 肠道激素途径﹕SCFAs促进L细胞分泌GLP-1和PYY﹐前者延缓胃排空、作用于下丘脑抑制食 欲﹐后者抑制下丘脑促进食欲的NPY神经元。
2) 神经递质途径﹕菌群产生GABA﹙抗焦虑﹚﹑调节色氨酸代谢影响5-HT﹙抑制食欲﹚﹐从而影响 情绪和与情绪相关的进食行为。
3) 迷走神经途径﹕菌群代谢产物可直接激活迷走神经传入纤维﹐快速传递饱腹感信号至大脑。
2.5 食欲与饱腹感的神经内分泌调控(二)
脑饥饿型的核心是饱腹感信号传导障碍(GLP-1/PYY不足或中枢抵抗)﹐情绪饥饿型的核心 是奖赏通路和情绪调节系统异常﹙5-HT/GABA失衡﹚。
2.6 能量消耗与产热的菌群调控
菌群通过激活棕色脂肪和白色脂肪褐变来增加能量消耗:
1) 棕色脂肪激活﹕次级胆汁酸激活TGR5﹐启动cAMP-PKA通路﹐上调PGC-1α﹐驱动UCP-1表 达,增强产热;Akk菌及其代谢产物也能显著激活棕色脂肪。
2) 白色脂肪褐变﹕次级胆汁酸、SCFAs可通过激活交感神经、促进M2型巨噬细胞浸润等途径, 诱导白色脂肪转化为米色脂肪,表达UCP-1。
3) 线粒体活性增强﹕丁酸等SCFAs通过抑制HDAC、激活AMPK,上调PGC-1α,全面提升细 胞产热能力。
低代谢型肥胖者肠道中Akk菌等产热相关菌群缺失,丁酸和次级胆汁酸产生不足,导致AMPK、 PGC-1α、TGR5等产热通路激活障碍。
2.7 抑制营养吸收
抑制营养吸收机制﹕通过调节宿主脂肪酶活性及胆盐水解酶分泌,从源头阻断脂质乳化与转运 蛋白表达。同时,利用特定菌群产生的抑制剂,直接下调α-淀粉酶活性;配合短链脂肪酸酸 化肠道环境,有助于减少热量摄入。
PART 3 益生菌靶向菌群体重管理法
3.1 益生菌的定义与菌株特异性
根据WHO/FAO定义,益生菌是“当给予足够数量时,对宿主健康产生有益作用的活性 微生物”。益生菌的功效具有严格的菌株特异性,即使同一菌种的不同菌株,其功能也可能存 在显著差异。因此,在体重管理中,必须明确到菌株水平。
3.2 “靶向菌群体重管理法”的提出
基于肠道菌群调控体重的四大核心机制﹙修复屏障﹑调节胆汁酸﹑产生SCFAs﹑调控食欲﹚﹐万 益蓝WONDERLAB在营养学﹑微生态等多学科专家指导下,提出“靶向菌群体重管理法”—— 针对特定代谢缺陷,补充具有明确功能特性的特定益生菌菌株,实现精准干预。
该方法构建了包含三个核心方面的综合干预体系:
1) 修复肠道屏障和改善炎症:为整个干预奠定基础,减少内毒素易位,改善胰岛素敏感性。
2) 调节胆汁酸盐代谢:通过BSH活性菌株减少脂肪吸收,促进胆固醇消耗。
3) 促进SCFAs产生和改善饱腹感:刺激GLP-1等激素分泌,增强饱腹感,改善葡萄糖耐量。
通过这三大靶点﹐持续制造“能量摄入<能量消耗”的缺口﹐实现可持续的体重管理。
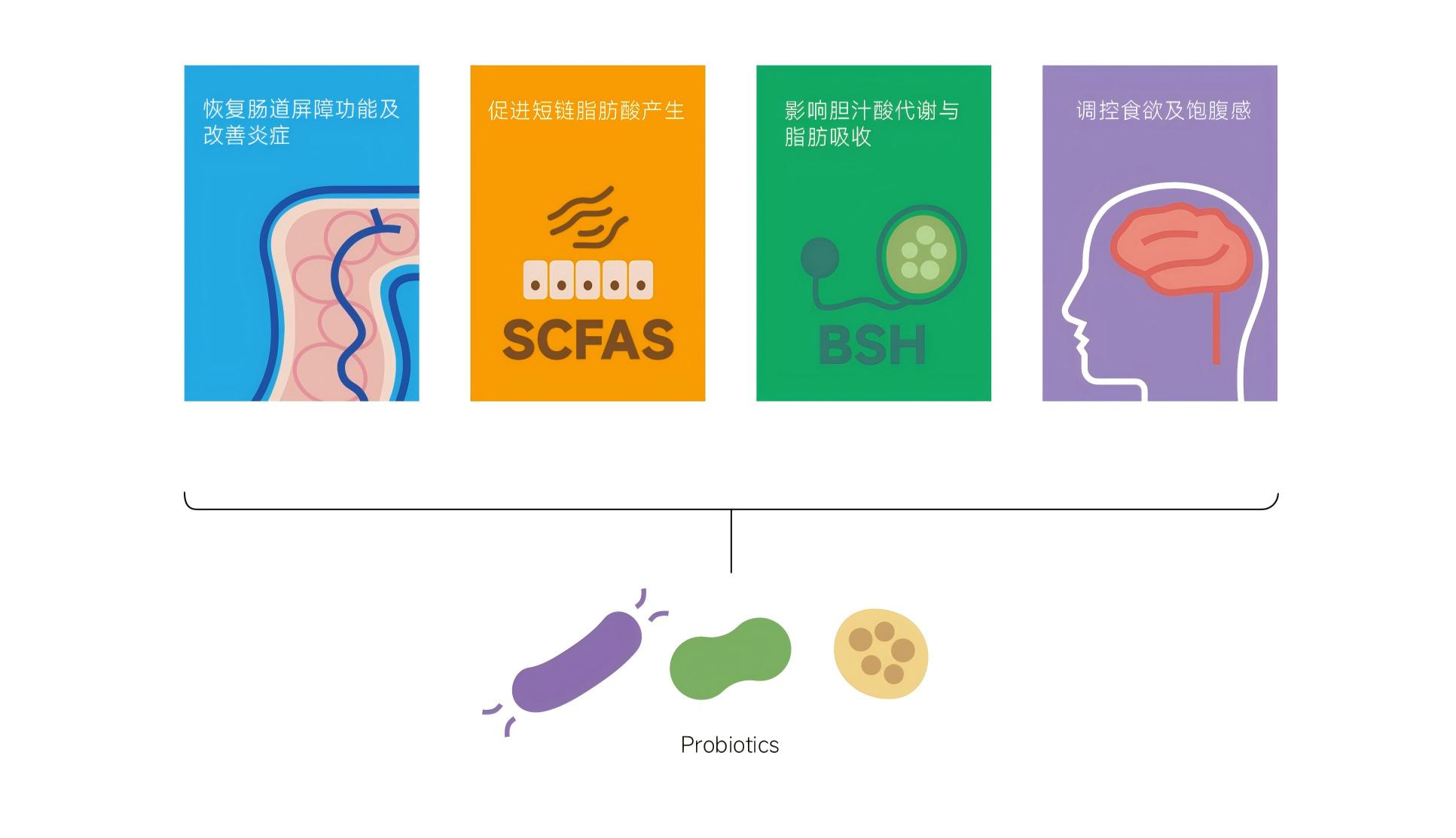
图 3 靶向菌群体重管理法
3.3 靶向菌群管理法的应用时序
科学的干预应遵循以下时序:
1) 肠道屏障修复﹙第 1-2 周﹚﹕建立健康的肠道微环境基础。
2) 改善肠道炎症(同步进行):降低慢性炎症对菌群定植的不利影响。
3) 改善菌群结构:通过多样化益生菌重建菌群平衡。
4) 促进有益菌稳定定植:确保长期效果。
5) 调节胆汁酸盐代谢:减少脂肪吸收。
增强饱腹感机制:减少能量摄入。
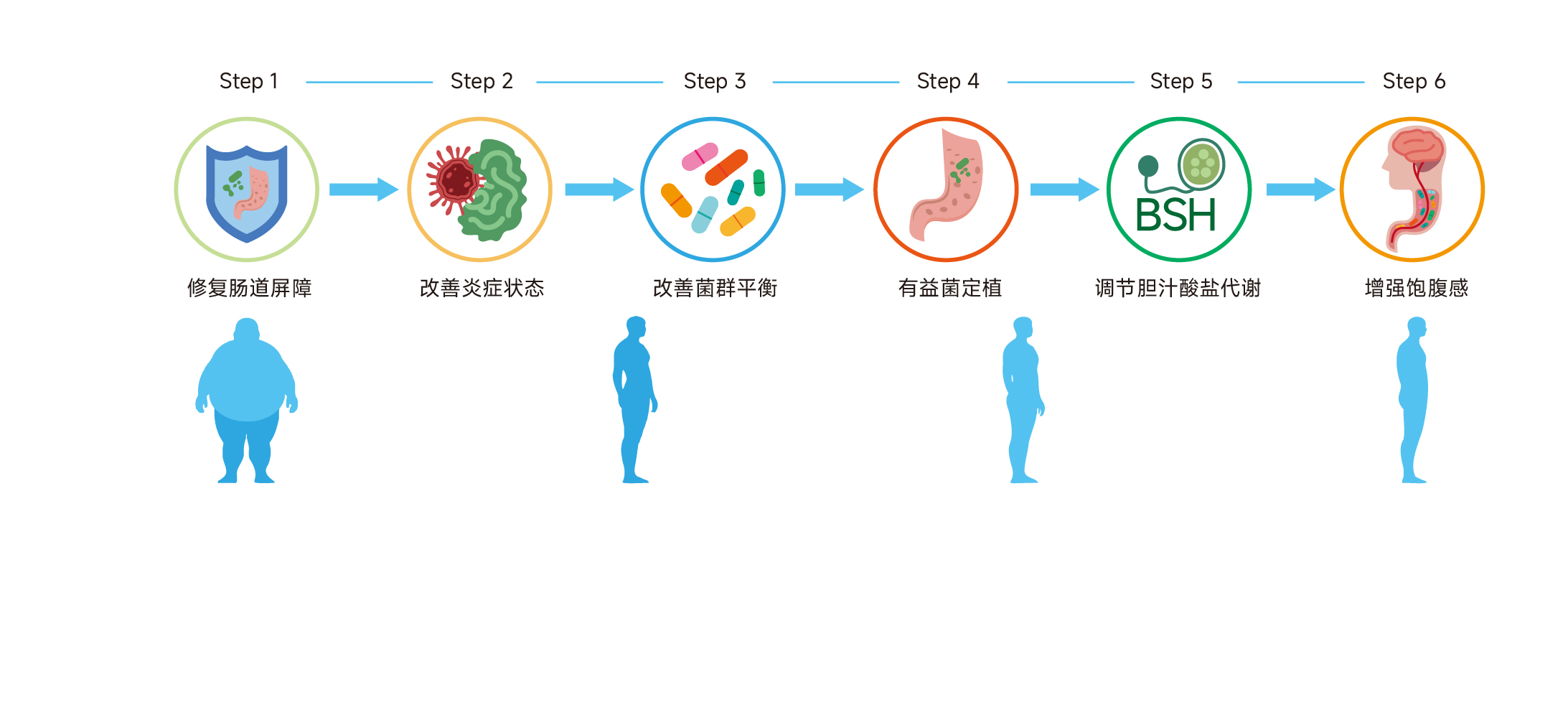
图 4 靶向菌群体重管理法实施的科学时序
3.4 基于肥胖分型的精准靶向干预策略
3.4.1 通用基础干预 ﹙所有分型的第 1-2 周)
核心机制:恢复肠道屏障完整性,降低代谢 性内毒素血症。
推荐菌株组合:
1) 鼠李糖乳杆菌GOLDGUT-M520: 显著 增加紧密连接蛋白ZO-1 ﹑ Occludin 表达﹐增 强NK细胞活性﹐提高 sIgA 水平。
2) 罗伊氏粘液乳杆菌 GOLDGUT-LR99: 恢复occludin和ZO-1 水平﹐降低TNF-α﹑ IL-6 等炎症因子。
3) 动物双歧杆菌乳亚种BB-12: 竞争性附着 于肠道上皮﹐产生乙酸﹐刺激 sIgA 分泌。 预期效果﹕肠道通透性显著降低﹐血清LPS 水 平下降﹐ CRP﹑ IL-6 等炎症标志物改善。
3.4.2 针对 “脑饥饿型” 的靶向干预
核心机制﹕调节肠 - 脑轴﹐恢复神经递质 平衡﹙ GABA ﹑ 5-HT ﹚﹐减轻神经炎症。
推荐菌株组合:
1) 罗伊氏粘液乳杆菌 GOLDGUT-LR99: 抗炎﹑促进色氨酸向5-HT 转化﹐改善情绪 状态。
2) 鼠李糖乳杆菌GOLDGUT-M520: 产 GABA, 调节免疫,保护神经系统。
预期效果:
1) 降低情绪化进食频率﹐改善焦虑与抑郁情绪。
2) 减少对高热量食物的渴望。
3) 通过迷走神经途径恢复饱腹感信号传导。
3.4.3 针对 “情绪饥饿型”的靶向干预
肠道菌群、情绪(如抑郁焦虑)与肥胖之间存在复杂的双向互动。肠道菌群失调通过免疫 炎症、神经递质及内分泌途径,引发代谢紊乱与心理失常。
1﹚ 机制联系:
•肥胖影响﹕ 菌群失调﹙如厚壁菌门比例升高)会增强能量提取,并产生脂多糖驱动慢性炎 症,干扰瘦素表达与产热作用,促进脂肪堆积。
•情绪调控﹕菌群通过“肠-脑轴”影响血清素、多巴胺等神经递质合成。菌群失调会降低海 马体神经营养因子﹙BDNF﹚水平,并因短链脂肪酸﹙SCFAs﹚减少导致HPA轴﹙压力系统﹚失调,使 皮质醇水平升高,引发焦虑与抑郁。
2﹚ 恶性循环﹕肥胖与抑郁常互为因果。肥胖导致的激素紊乱会改变菌群结构,破坏肠道屏障,激活压力反应。这种生理反馈与体重歧视带来的心理压力交织,加剧炎症与快感缺失,使 体重控制更加困难。
3﹚治疗前景:
•益生菌﹕ 调节菌群平衡可改善屏障功能,调节神经递质,缓解压力与抑郁。
•药物交叉﹕减重药物﹙如GLP-1激动剂﹚能改善菌群并减轻神经炎症;抗抑郁药也会改变菌 群构成,影响药物代谢。
总结﹕肠道菌群是连接代谢与精神状态的核心枢纽。维护肠道平衡对防治肥胖与情绪障碍具 有重要临床价值。
3.4.4 针对“胃肠饥饿型” 的靶向干预
核心机制﹕促进短链脂肪酸﹙SCFAs ﹚产生﹐刺激肠道 L 细胞分泌 GLP-1 和 PYY。
推荐菌株组合:
1)青春双歧杆菌 FJSSZ23M10:高效产 SCFAs ﹙丁酸﹑丙酸﹚ , 激活 FFAR2/3 ﹐促 进 GLP-1 分泌。
2) 鼠李糖乳杆菌D4-4 + 副干酪乳杆菌D3-5: 通过交叉喂养机制﹐显著提高肠道丁酸产量。
3) 产胞外多糖双歧杆菌﹕ EPS 作为益生元被 其他产SCFAs菌利用﹐间接提高SCFA水平。
预期效果﹕
1) 餐后饱腹感增强 30-50% ﹐饱腹感持续时 间延长。
2) 胃排空时间恢复至正常范围 (90-120 分钟)。
3) 自然减少每日能量摄 入300-400kcal。
3.4.5 针对“低代谢型” 的靶向干预
核心机制﹕调节胆汁酸代谢﹐促进能量消耗 和棕色脂肪产热。
推荐菌株组合:
1) 嗜酸乳杆菌GOLDGUT-LA100: 高BSH 活性﹐将结合型胆汁酸水解为游离型﹐促进 次级胆汁酸生成。
2)植物乳杆菌组合(CECT7527+CECT7528 +CECT7529): 增强 BSH 活性,降低胆固 醇﹐激活 TGR5。
3)Akkermansia muciniphila(Akk菌﹚﹕激活棕色脂肪产热﹐上调 UCP-1 表达,增加 能量消耗。
预期效果﹕
1) 基础代谢率提升 5-10%。
2) 脂肪吸收效率降低10-15%。
3) 总胆固醇下降10-15% ﹐ LDL-C下降15- 20% ﹐甘油三酯下降 20-30%。
4) 腰围、体脂率显著下降。
PART 4 结论与展望
靶向菌群体重管理法作为创新性的体重管理策略﹐基于肠道菌群与宿主代谢健康的深度关联﹐ 突破传统减重“单一能量负平衡” 的局限。
其核心优势在于﹕
1) 精准性﹕强调益生菌功效的菌株 特异性,针对不同代谢环节选择特定菌株。
2) 系统性﹕多靶点协同干预,同时作用于屏障修 复、代谢调节、脂质吸收、炎症改善和食欲控制,构建完整的生物学干预网络。
3) 可持续 性:通过重建健康的肠道微生态,从根本上改变宿主代谢模式,实现长期效果。
4) 安全性: 天然益生菌,具有良好的生物相容性,适合长期应用。随着精准医学理念的深入和肠道微 生态研究的深化,靶向菌群体重管理法正迎来前所未有的发展机遇。
未来,该方法将从相 对粗放式应用向真正的个体化精准干预转变,通过多组学技术、人工智能辅助分析和更精 准的菌株筛选,为不同个体提供量身定制的体重管理解决方案。我们期待这一创新方法在 全球肥胖防控体系中发挥越来越重要的作用,为人类健康事业做出重要贡献。